17 декабря 2006 г. в Московском инженерно-физическом институте (МИФИ) проходила традиционная олимпиада по физике памяти профессора Игоря Владимировича Савельева. И.В.Савельев в течение многих лет был заведующим кафедрой общей физики МИФИ, он является автором ряда классических учебников и задачников для студентов-физиков. Эти книги используются в качестве основного учебника в российских технических вузах, переведены на многие иностранные языки и являются настольными книгами молодых физиков во всем мире.
Олимпиада памяти И.В.Савельева традиционно проводится в середине декабря в МИФИ. Эта олимпиада является одним из туров Всероссийской физико-математической олимпиады Федерального агентства по атомной энергии (Росатома), которая проводится в несколько туров в течение всего учебного года в Москве (в МИФИ) и ряде крупных центров Росатома (г. Саров, г. Снежинск и др.) для школьников 11-х классов. Победители и призёры олимпиады Росатома (около 10% участников) получают существенные льготы при зачислении в МИФИ. Подробности об олимпиаде Росатома 2007/2008 уч.г. можно узнать по телефону приёмной комиссии МИФИ: (495) 324-84-17 и на сайте приёмной комиссии МИФИ: http://www.priem.mephi.ru.
На олимпиаде памяти И.В.Савельева в 2006 г. школьникам были предложены пять задач различной степени сложности. Ниже приводится вариант задания олимпиады и его подробное решение.
Вариант задания олимпиады
1. Ускорение свободного падения на поверхности некоторой планеты равно g = 16 м/с2, на высоте h = 1000 км от поверхности – g1 = 9 м/с2. Найдите радиус планеты.
Решение
Основная идея решения задачи заключается в том, что ускорение свободного падения на той или иной высоте определяется силой гравитационного притяжения тела к планете. Используя закон всемирного тяготения, получаем для ускорения свободного падания на поверхности планеты и на высоте h от поверхности
![]()
где G – гравитационная постоянная, M и R – масса и радиус планеты. Деля первое уравнение на второе и решая полученное уравнение, находим:
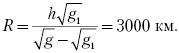
2. Из точки, находящейся на
высоте H над землёй, через равные промежутки
времени из состояния покоя падают маленькие
шарики. К тому моменту, когда седьмой шарик
начинает падение, первый падает на землю. Найдите
расстояние между вторым и четвертым шариками в
этот момент. Сопротивлением воздуха пренебречь. 
Решение
За то время, пока первый шарик долетит
до земли, начинают падать ещё шесть шариков (см.
рисунок). Следовательно, время падения первого
шарика на землю равно шести интервалам ![]() t между
падениями любых двух соседних. Поэтому интервал
t между
падениями любых двух соседних. Поэтому интервал ![]() t можно найти,
разделив время падения первого шарика на шесть. А
поскольку время свободного падения тела из
состояния покоя с высоты H составляет
t можно найти,
разделив время падения первого шарика на шесть. А
поскольку время свободного падения тела из
состояния покоя с высоты H составляет ![]() то
то
![]() (1)
(1)
Теперь найдём координаты второго и четвертого шариков в момент падения первого на землю. Для этого заметим, что зависимость координаты х каждого шарика от времени (ось X показана на рисунке) имеет вид
![]() (2)
(2)
где время t отсчитывается от
момента начала падения этого шарика, и что второй
шарик будет двигаться к моменту падения первого
шарика на землю в течение пяти интервалов ![]() t (1), а
четвертый – в течение трёх (см. рисунок).
Подставляя эти значения времени в зависимость (2)
и используя формулу (1), получаем координаты
второго и четвёртого шариков в момент падения
первого на землю:
t (1), а
четвертый – в течение трёх (см. рисунок).
Подставляя эти значения времени в зависимость (2)
и используя формулу (1), получаем координаты
второго и четвёртого шариков в момент падения
первого на землю:
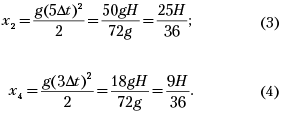
Вычитая теперь координату четвёртого шарика (4) из координаты второго (3), находим расстояние между вторым и четвёртым шариками в момент падения первого на землю:
![]()
3. В сосуде объёмом V0 при температуре T0 и давлении p0 находился воздух, содержащий некоторое количество озона O3. С течением времени озон полностью превратился в молекулярный кислород. Получившийся воздух при температуре T и объёме V оказывает то же самое давление p0, что и первоначальная смесь газов. Найдите первоначальное число молей озона в сосуде.
Решение
Пусть первоначально в сосуде
содержалось ![]() молей
озона и
молей
озона и ![]() 1
молей всех остальных газов. Тогда закон Дальтона
для первоначальной смеси газов даёт
1
молей всех остальных газов. Тогда закон Дальтона
для первоначальной смеси газов даёт
![]() (5)
(5)
где R – универсальная газовая постоянная. Поскольку при химической реакции распада озона
2O3 = 3O2, (6)
из каждых двух молекул озона
образуются три молекулы кислорода, то из ![]() молей озона
получается 3
молей озона
получается 3![]() /2
молей кислорода. Поэтому закон Дальтона для
смеси газов после полного распада озона при
новых температуре и объёме даёт
/2
молей кислорода. Поэтому закон Дальтона для
смеси газов после полного распада озона при
новых температуре и объёме даёт
![]() (7)
(7)
Вычитая из формулы (7) формулу (5) и решая полученное уравнение, находим:
![]()
_____________________________________
Сергей Евгеньевич Муравьёв, заместитель заведующего кафедрой теоретической физики МИФИ, к.ф.-м.н., доцент.
Окончание cм. в № 6/08