ПредисловиеПредставленный учебный web-ресурс по молекулярной физике, состоящий из семи уроков, предназначен для учащихся 10-х классов средних общеобразовательных школ, являющихся пользователями персональных компьютеров. Его могут также использовать абитуриенты и слушатели подготовительных курсов вузов. Вы можете ознакомиться с содержанием уроков, а затем приступить к их изучению, начиная с первого и решая указанные задачи. Приведен список литературы, CD-ROM по физике, список Web-ресурсов по физике и ссылки на сайты дистанционного образования. Имеются задачи повышенной трудности для тех, кто хочет лучше понять физику. Для обратной связи можно использовать Гостевую книгу, форум и E-mail. Желаю вам успехов в дистанционном изучении молекулярной физики!
Учитель физики и информатики школы № 1126, Львовский Марк Бениаминович, г. Москва.E-mail: marklv25@mtu-net.ru |
|
|
Содержание
|
Список литературы и использованных материалов
|
|
Урок 4. Идеальный газ. Основное уравнение МКТИзвестно, что частицы в газах в отличие от жидкостей и твердых тел располагаются друг относительно друга на расстояниях, существенно превышающих их собственные размеры. В этом случае взаимодействие между молекулами пренебрежимо мало и кинетическая энергия молекул много больше энергии межмолекулярного взаимодействия. Для выяснения наиболее общих свойств, присущих всем газам, используют упрощенную модель реальных газов – идеальный газ. Основные отличия идеального газа от реального газа:
Реальные разреженные газы
действительно ведут себя подобно идеальному
газу. Воспользуемся моделью идеального газа для
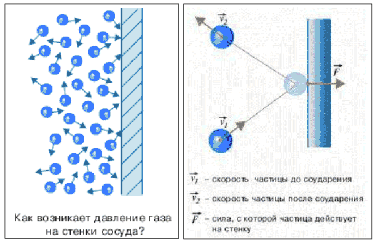
объяснения происхождения давления газа.
Вследствие теплового движения частицы газа
время от времени ударяются о стенки сосуда. При
каждом ударе молекулы действуют на стенку сосуда
с некоторой силой. Складываясь друг с другом,
силы ударов отдельных частиц образуют некоторую
силу давления, постоянно действующую на стенку.
Понятно, что чем больше частиц содержится в
сосуде, тем чаще они будут ударяться о стенку
сосуда, тем большей будет сила давления, а значит,
и давление. Чем быстрее движутся частицы, тем
сильнее они ударяют в стенку сосуда. Мысленно
представим себе простейший опыт: катящийся мяч
ударяется о стенку. Если мяч катится медленно, то
он при ударе подействует на стенку с меньшей
силой, чем если бы он двигался быстро. Чем больше
масса частицы, тем больше сила удара. Чем быстрее
движутся частицы, тем чаще они ударяются о стенки
сосуда. Итак, сила, с которой молекулы действуют
на стенку сосуда, прямо пропорциональна числу
молекул, содержащихся в единице объема (это число
называется концентрацией молекул и обозначается
n), массе молекулы m0, среднему квадрату их
скоростей и площади стенки сосуда. В результате
получаем: давление газа прямо пропорционально
концентрации частиц, массе частицы и квадрату
скорости частицы (или их кинетической энергии).
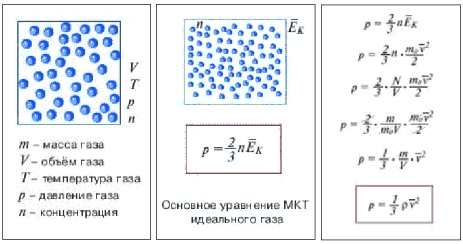
Зависимость давления идеального газа от
концентрации и от средней кинетической энергии
частиц выражается основным уравнением
молекулярно-кинетической теории идеального
газа. Мы получили основное уравнение МКТ
идеального газа из общих соображений, но его
можно строго вывести, опираясь на законы
классической механики. Иллюстрации Основные итоги |
|

|
|
|
|
Урок 1. Основные положения молекулярно-кинетической теорииМолекулярно-кинетическая теория (МКТ) занимается изучением свойств веществ, основываясь при этом на представлениях о частицах вещества. МКТ базируется на трех основных положениях:
Беспорядочное (хаотичное) движение атомов и молекул в веществе называют тепловым движением, потому что скорость движения частиц увеличивается с ростом температуры. Экспериментальным подтверждением непрерывного движения атомов и молекул в веществе является броуновское движение и диффузия.
|
|
Задачи к уроку 4 (в порядке нарастающей сложности) |
|
| Задача 1. Как изменится давление водорода, находящегося в закрытом сосуде, если каждая молекула распадется на отдельные атомы, а средние квадраты скоростей не изменятся? | |
| Задача 2. Имеются два одинаковых сосуда. В одном из них находится кислород, а в другом – азот. Число молекул каждого газа и средние квадраты их скоростей одинаковы. Давление кислорода равно 32 кПа. Чему равно давление азота? | |
| Задача 3. В результате нагревания газа в закрытом сосуде средняя квадратичная скорость молекул увеличилась в 2 раза. Как изменилось давление? | |
| Задача 4. В сосуд, содержащий некоторое количество атомов гелия, добавляют такое же число молекул водорода, имеющих среднюю кинетическую энергию теплового движения, равную средней кинетической энергии теплового движения атомов гелия. Во сколько раз изменится давление в сосуде? | |
| Задача 5. Рассчитайте силу удара молекулы газа о стенку сосуда, если она движется перпендикулярно стенке со скоростью u, масса молекулы m0, а время ее соударения со стенкой dt. | |
| Задача 6. Сколько ударов Z молекул о стенку площадью S = 1 м2 происходит за 1 с? | |
 Задача 7 (проблемная).
Спутник объемом V = 1000 м3 заполнен гелием.
Метеорит пробил в стенке спутника отверстие
площадью S = 1 см2. Оцените время, за которое
давление упадет на 1%. Температуру внутри
спутника считать неизменной. Средняя
квадратичная скорость атомов гелия v = 500 м/с. Задача 7 (проблемная).
Спутник объемом V = 1000 м3 заполнен гелием.
Метеорит пробил в стенке спутника отверстие
площадью S = 1 см2. Оцените время, за которое
давление упадет на 1%. Температуру внутри
спутника считать неизменной. Средняя
квадратичная скорость атомов гелия v = 500 м/с. |
|
  |
|
 
|
|

|
|